我國(guó)慢性腎病患者高達1.2億人,已發(fā)展成(chéng)終末期腎病患者有200萬,目前僅有30多萬人接受透析治療,治療率僅爲15%,遠低于歐美國(guó)家的90%。中國(guó)血液透析市場主要由德國(guó)費森尤斯、日本尼普洛等占據,血液透析行業的市值約爲1000億-1400億人民币,是中國(guó)最具潛力的藍海市場之一。血液透析符合《“健康中國(guó)2030”規劃綱要》等國(guó)家政策,具有制備技術壁壘高、多學(xué)科交叉等特點。血液透析器是人工腎系統的核心元件。尿毒症患者需要終生透析,随著(zhe)我國(guó)進(jìn)入老齡化社會,以及城鄉居民大病保險試點政策的啓動推廣,我國(guó)對(duì)血液透析器的需求將(jiāng)出現井噴式增長(cháng)。因此研發(fā)具有自主知識産權的高性能(néng)透析膜/器具有重要的民生和社會意義。
常用的血液透析聚合物膜,由于血液相容性較差,在與血液接觸時,會引發(fā)血小闆的粘附、聚集和釋放反應,導緻凝血機制異常造成(chéng)凝血及血栓等臨床反應。而目前臨床上常用的抗凝手段主要是直接注射抗凝劑(如未分級肝素及低分子量肝素),起(qǐ)到抗凝血、抗血栓等多種(zhǒng)功用。然而大量肝素的使用往往會加大患者的出血風險。并且肝素長(cháng)期依賴也會導緻血小闆減少症(HIT)、皮膚反應、血漿脂解活性的抑制、嗜酸粒細胞增多、高鉀血症、骨質疏松等副作用。因此如何發(fā)展自抗凝透析器,實現無肝素透析是目前血液透析的發(fā)展趨勢。
中國(guó)科學(xué)院甯波材料技術與工程研究所先進(jìn)功能(néng)膜團隊于2014年開(kāi)始進(jìn)行透析膜方面(miàn)的研究,并于近期取得了系列進(jìn)展。
1)膜微孔結構調控:發(fā)展了一種(zhǒng)生物相容性良好(hǎo)的聚乳酸血液透析膜,并系統探索了聚乳酸膜的相轉化結構調控機理。可實現海綿狀孔/指狀孔等梯度結構有效調控(Journal of Membrane Science 2015, 478, 96-104),并且針對(duì)聚乳酸微孔膜結晶度低和耐熱性差的問題,發(fā)展了界面(miàn)交聯誘導結晶的方法,提高了微孔膜的結晶度及耐熱溫度(Journal of Membrane Science 2016, 513, 166-176,ACS Biomaterials Science & Engineering 2016, 2 , 2207–2216)。
2)膜表面(miàn)抗凝分子修飾:通過(guò)膜表面(miàn)多巴胺固定肝素(Journal of Membrane Science 2014, 452, 390-399)、膜表面(miàn)兩(liǎng)性離子化(Journal of Membrane Science 2015, 475, 469-479)、表面(miàn)PEG化(ACS Applied Materials & Interfaces 2015, 7, 17748-17755)、膜表面(miàn)水蛭素修飾(Journal of Membrane Science 2017, 523, 505-514)改善聚乳酸微孔膜的親水性及血液相容性,揭示了膜表面(miàn)親水抗蛋白吸附和類肝素抗凝分子抑制凝血瀑布效應的機理。
3)自抗凝透析器:中空纖維透析器内含超過(guò)1萬根中空纖維膜,其内徑通常小于200微米,在微米級的限域通道(dào)内實現親水和抗凝分子的修飾具有非常大的挑戰性。目前臨床用的聚砜和聚醚砜類透析器通常采用在相轉化過(guò)程中共混高分子量聚乙烯吡絡烷酮(PVP)實現其親水抗凝修飾,但是PVP與聚砜或聚醚砜存在相容性差異,通常易在膜表面(miàn)析出形成(chéng)“布丁”粒子,在透析過(guò)程中形成(chéng)挂血點,并容易進(jìn)入血液當中。針對(duì)該問題,研究團隊發(fā)展了一種(zhǒng)基于微孔膜的Top-down遷移及界面(miàn)交聯功能(néng)化策略(Journal of Membrane Science 2016, 520, 769-778,Journal of Membrane Science 2016, 513, 166-176),實現了抗凝分子在微孔膜表面(miàn)的修飾,進(jìn)一步地通過(guò)可控聚合技術合成(chéng)了具有親水基團(乙烯基吡咯烷酮)和抗凝基團(磺酸基團和羧酸基團)、具有序列排列結構的共聚物,通過(guò)微流控技術實現抗凝聚合物在透析器限域通道(dào)内的均勻分布,及界面(miàn)交聯固定,最終通過(guò)親水基團的抗蛋白吸附以及磺酸羧酸基團的抗凝機理協同提高透析器的血液相容性,如圖1-3所示,實現了整支透析器的自抗凝修飾,模拟透析實驗表明自抗凝透析器具有良好(hǎo)的中小分子清除性能(néng),具有潛在的臨床應用前景。上述工作作爲邀請論文發(fā)表在Journal of Membrane Science 2018, 563, 115-125。
上述研究得到國(guó)家自然科學(xué)基金(51473177),中科院青年創新促進(jìn)會(2014258),甯波市生命健康重大項目(2017C110034)的資助支持。

圖1 自抗凝透析器及膜表面(miàn)抗血小闆吸附
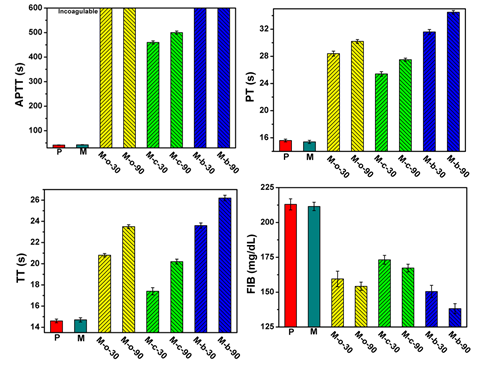
圖2 自抗凝透析膜表面(miàn)凝血四項指标:APTT(活化部分凝血活酶時間),PT(凝血酶原時間),TT(凝血酶時間)和FIB(纖維蛋白原),其中APTT超過(guò)600s,表現出高抗凝特性

圖3 自抗凝透析膜内外表面(miàn)形貌
(高分子事(shì)業部 劉富)
